〈有機化学の基礎編(その2)〉
③ アルケン類(電子軌道論)
電子を媒介にした「共有結合」など宇宙には存在せず、化合結合の実態とは外殻電子の軌道磁界の「磁極結合」に基づくものだというのが銀河一般科学の常識です。では「磁極結合」という宇宙理論で万物の結合状態を本当に矛盾なく説明できるのでしょうか。不飽和炭化水素の中には炭素原子同士の「二重結合」を有する「アルケン類」や、あるいは「三重結合」を有する「アルキン類」などの化合物も在って、またベンゼンの様な不飽和の環式化合物なども存在します。中には現行の結合理論では説明が困難な場合も多く、そうした難解な現象ですら納得が行く説明ができなければ科学者の支持は得られないと思います。別に科学者の支持など我々には必要ありませんが、真実の理論が分かれば何事も本物の技術が育まれて、新しい発見や発明や開発が可能になるからです。理論など所詮は「実践の踏み台」に過ぎず、応用実践で証明できるか否か、それが問題なのです。つまり、科学研究も野球と一緒であって、「結果」が出せるか否か、それが重要なのです。
とはいえ、大基礎の理論を踏み間違えてしまえば盲目の海を航海する嵌めとなり、MHD発電機や粒子コライダーや高温核融合炉の如く、あるいは癌遺伝子研究やiPS細胞研究の如く、意味の無い基礎研究をひたすらに続けるだけの話、1000年の時間を費やしても、いや1万年の時間を費やしても、1cmの成長も無ければ、また一欠片(ひとかけら)の実績も得られないものです。間違った理論は遅かれ早かれいつか正す必要があるものと思います。原子の化学結合は電子の公転運動が描く軌道磁界で決定されるもので、共有結合という既成概念はその根底から覆される事になり、新たな結合概念を最初の一から勉強し直す必要があります。ここでは先ず、アルカンの炭素鎖の「単結合」と、アルケンの「二重結合」と、アルキンの「三重結合」の原子構造に関して説明していきたいと思います。アルカン類のエタン(CH3CH3)を例に挙げれば、その構造様式とは下記(1図)の様になります。

そもそもエタン(C2H6)とはメタン(CH4)ガスの合体物と言っても良い存在であり、2個のメタン分子が互いに向き合って、片方が逆様状態で合体した物と言えば、おおよその構造様式を理解できると思います。メタン分子に頭側と足側という規定があるのかと言えば、実は元素には全て上下の区別が存在し、基本的には炭素原子の1s電子軌道が「赤道面」を呈しており、そのN極側が頭部、反対のS極側が脚部になります。球体を呈する物は全て、つまり天体でも細胞でも分子も元素も粒子も全て上下左右と裏表は存在しており、物質生命と言えども基本的に生命である事には変わりはありません。1図に示したエタンの炭素鎖は基本的に「単結合」で結ばれており、アルカン類の炭素鎖の基本的な構造を表しています。単結合の炭素鎖は隣同士が交互に逆向きに向き合った状態で鎖を形成しています。下記(2図)は1図の原子模型であり、電子軌道が描かれた詳細図です。二重結合の場合は「なるほど」と文字通りに納得できますが、三重結合の場合は実際に三重になって結ばれている訳ではなく、特殊な結合状態を表しています。地球化学も三重結合の説明に困難を呈している様ですが、そもそも三重結合などという結合様式は存在しない事を認識して頂きたいと思います。



有機化学の予備知識が無い人には上記の図も一体何を示しているのか良く分からないと思いますが、物質の成り立ち構造がちゃんと理解できないと物質操作がままならず、「どうしてこんな特殊な物質を宇宙人達は作り出せるのだろう」と考え込んでしまうかもしれませんね。有機化学の前提になるのが「電子軌道論」であり、地球の場合は量子力学が台頭してくる以前の昔の電子論に一度戻す必要があります。原子核を周回する軌道電子は何重にも原子核の周囲を層状に取り巻いており、それらの軌道磁界の役割とは基本的に食糧(気の粒)と運動エネルギー(光波動)を外界から獲得して原子核へ送付する為の手段だと言えます。外殻電子の供給は原子核が内蔵する電子群で賄(まかな)われており、また外殻電子は外界の環境次第でいつでも原子核へ戻る事ができます。原子核反応を突き詰めて研究していくと、原子とは「まるで生き物だ」と痛感せざるを得なく、単なるパチンコ玉状の物体であるとは「とても思えない」というのが私の実感でしょうか。
炭素原子の軌道電子配置は「[He]2S2・2P2」なので、S軌道と同じ平面に位置するPz軌道が赤道面となり上下を規定していますが、それと垂直に交わるPy軌道が左右を規定しています。また陰電子は原子核に対して必ず「反時計回り」で公転をしているので、そうした常識的な基礎知識は記憶に残して頂きたいと思います。原子核の内軌道を周回するS軌道電子は大概の場合は同一軌道内に電子(e-)を2個入れて、片方を逆様状態(極性が逆)にして、互いの中心磁束流で結ばれた状態で公転運動をしています。この様な軌道磁界(電子が2個入っている)は「閉塞場」を呈しており、軌道磁界そのものに極性が形成されず、その為に化学反応を起こす事ができません。化学反応を唯一起こせる軌道磁界とは1個の電子が軌道を周回している場合のみです。当然、S軌道電子の外側を周回するP軌道電子も理屈は一緒、一つの電子軌道に2個の電子が入れば、P軌道磁界は閉塞場となって化学反応に加わる事はできません。地球ではこの現象を「パウリ禁制」と呼んでいる様ですが、これは当たり前の常識でしょうか。
外殻電子は基本的に原子核を構成する「陰子(イントロン)」が放っており、電子(e-)を放った陰子は陰電荷を失って「中性子(ニュートロン)」に変化します。しかし、電子の母親である中性子はいつだって電子を呼び戻す事が可能であり(原子核のK電子捕獲現象)、電子を吸収した中性子は再び陰子へと戻って電荷を有する事になります。大きな元素の原子核は内核と外核に分かれており、内部には無電荷のD-重合体分子(ヘリウム核)が存在します。原子番号が18番目のアルゴン原子(Ar)以上の元素から原子核の内部に無電荷粒子を備えている元素が出現する事になり、特にチタン(Ti)以上の金属元素の大半は一つ以上の無電荷粒子を備えている事になります。ちなみに、無電荷粒子はヘリウム原子核単位なので質量数は4(陽子2+陰子2)を呈示しますが、互いの電荷量そのものが相殺されている為に、一見は中性子に見えます。地球の核物理学者は100種の元素など今更調べようが無いくらい研究し尽くしたと思っている様ですが、我々から言わせて貰えば「まだ何も分かっていない」と言わざるを得ません。
電子軌道磁界は「磁場」と「力場」の両方の機能を有しており、当然「双極子モーメント」を有しています。化学反応に関しては単独電子を有する一番外側の軌道磁界が実権を握っていますが、一般的な話をすれば、電子の軌道磁界のお陰で我々は大地に吸収される事なく磁気的な反発力によって歩行が可能であると言えましょう。万物の形状は電子の軌道磁界によって具現し、それによって維持されており、あなたが鉛筆を握れるのも、あるいは食事ができるのも、はたまた空気を吸えるのも全て軌道磁界のなせる「技」なのです。電子の軌道磁界を持たない物質を我々は「アストラル物質」と総称していますが、電磁的な反発力が無い理由から、物質世界の中を抵抗無くスルッと通り抜けてしまう事ができます。従って、電子の軌道磁界に関する知識は極めて重要なものであり、日常生活とは無縁な専門的な話をしている訳では決して無いのです。
さて、ラザフォードやボーアの原子模型の時代(1913年)の話に遡りますが、原子核を取り巻く電子層の収納帯(電子殻)を区分けして、K核から始まって、L殻、M殻、N殻、O殻、P殻までの収納帯に分割しました。当時は電子が原子核の周囲を公転運動(軌道運動)していると考えられていましたが(初期量子力学)、その後はシュレーディンガーの波動関数を導入し、またボルンの電子の存在確率解釈などが用いられて、数学者が主導する新しい量子力学では電子の軌道運動が誤った解釈であると決定されてしまいました。彼等は電子は原子核を通り抜けて激しく振動しており、確率でなければ存在位置を示せないと言うのです。これはオリオンスイーパー達の魔手によって真理が捻じ曲げられてしまった瞬間でしょうか。電子が軌道運動をしている事は確かな事実なのですが、問題は現象を正確に捉えた正しい解釈がおぼつかなかった事であり、自然界の道理を飛び越えた人間の空想話を真実化させて、それを数理で無理やり押し通して詭弁化した事でしょうか。数学者は道理よりも数理を基軸にして思考するから浅慮な単細胞頭となり、発想力が小学生の如く貧弱になるのです。
100種の元素の母体は「星のコア」であり、いわゆる「D-重合体」が分解して発生してきたものですが、原子番号が20以下の小さな元素に関しては母星のコアではなく、その大半が星間物質であって、「岩石渦」と呼ばれる小さな渦巻のコアが分解して誕生してきたものです。原子の電子軌道は自然原理に基づいて配置が定められており、大きな原子の電子軌道は、円筒状に原子核を包み込む「7つの軌道(f軌道)」と、まるで渦巻の様に平面的に原子核を取り囲む「5つの軌道(d軌道)」と、襷(たすき)掛けの様に原子核を包み込む「3つの軌道(p軌道)」と、原子核の赤道周囲に位置する「1つの軌道(s軌道)」という四種類の軌道形態があります。原子核から外界へ放たれた電子は自然にその電子軌道を周回する事になります。これらの電子軌道は渦磁場に刷り込まれた粒子の原子本能と言っても構わないものであり、当然、自然界の運動原理ですから数式でも簡単に表現できますが、実際には「f軌道」以上の電子軌道は存在しません。

窒素原子(N)の電子軌道は一般に[He]2s2・2p3と表現できますが、それを原子構造で示すと下図(4図)の様になります。最外殻のp軌道に3個の電子を配置させた窒素原子の原子価は、いわゆる6本の反応手を保有する事になり、結合手を多く備えている理由から有機物の立体骨格には欠かせない存在と言えます。また窒素原子核は核子数が14個であり、核スピン量が1である事実を考えれば、元々の原子核の構成が「陰子が7個」で「陽子が7個」である事が分かります。核スピン量が1であるという事は、原子核の中心点でデュートロン(重水素原子核: Du単位)が1個スピンしている事になりますので、残りの核子構成は「ヘリウム原子核単位(He単位)」が3組である事が分かります。つまり、窒素原子核は3組のHe単位に囲まれた真ん中に一つのDu単位が存在し、それが原子核スピンをもたらしていると想定できる訳です。ちなみにHe単位はスピン量が相殺されており、全体としての回転はしていません。この様に思考分析していくと、3組のHe単位から構成される炭素原子核や、4組のHe単位から構成される酸素原子核はスピン量がゼロの安定原子核を呈しており、窒素原子核が非常に不安定である事が分かります。


磁極結合という観点から原子価を考えれば、水素は2価、炭素は4価、窒素は6価、酸素は4価であり、それぞれの最外殻の反応軌道磁界は水素(1s)、炭素(2pzと2py)、窒素(2pzと2pyと2px)、酸素(2pyと2px)となります。ちなみに、酸素の2pz軌道には2個の電子が入力しており閉塞場を呈しています。また核スピンの話ですが、水素原子核とは陽子の事ですから、当然、スピン量は素粒子共通の1/2スピンを呈しており、水素と窒素の原子核はそれ自身が回転している事になります。原子核が抱える陰電子数(e-)は基本的にそれを産出する「陰子数」と一致しており、また陽子が抱える陽電子数(e+)とも一致しているのが普通です。陰子が外に陰電子を放てば、陰子は電荷を失い中性子化してしまいますが、その分軌道磁界が形成されて、原子核はより大きな外磁場を有する事になります。小さな原子核を有する原子は小さな外磁場しか囲えず、自己の命を保持する為の気の粒も光エネルギーも不足しがちですが、一方、大きな原子核を有する原子は働き手(陰電子の事)を複数備えており、何重にも堅固な砦を築いて大量の気の粒や光エネルギーを確保する事ができます。
単独電子が周回する軌道磁界は必ずN極とS極という両方の触手を備えており、N極側とは磁束が吹き出す「作用手(能動手)」であって、また、S極側とは相手の磁束を受け入れる「引き手(受動手)」を意味しています。酸素原子は4価で窒素原子は6価の触手を保有していますが、普段はN極側の作用手の方で仕事をする事から、酸素は2価、窒素は3価として知られていますが、相手が逆に作用を仕掛けてくる場合はS極側で対応する為に、原子価が増える事になります。ただ、幾つかの例外があって、イオウ原子(S)などの場合は、[Ne]3s2・3p4の電子構造であり、一つのp軌道が充足されて閉塞状態である事から、普段は酸素原子と同じ4価を呈していますが、水溶液の中でイオン化し、軌道電子を1個手放す(水六員環に電子を奪われる)場合があります。そういう場合は閉塞が解けたp3軌道となり、pz軌道とpy軌道とpx軌道に1個ずつ電子が配置される事になります。従って、4価の筈のイオウ原子が6価の触手を持つ事になります。

また、鉄原子(Fe)の様な平面的な渦軌道(d軌道)を取る元素の場合は、鉄の軌道式はFe=[Ar]3d6・4s2になりますが、実際の構造式はFe=[Ar]4s2・3d6であって、d軌道の方がs軌道よりも外側に位置しています。実はこれ、3d軌道を有するスカンジウム(Sc)、チタン(Ti)、パナジウム(V)、クロム(Cr)、マンガン(Mn)、鉄(Fe)、コバルト(Co)、ニッケル(Ni)といった元素は皆一緒であり、3d軌道が充足した(3d10)元素である銅元素(Cu)から始めて、d軌道の外側に4s軌道が配置される事になります。鉄原子は本来、一番外側のd軌道に6個の電子を配置させていて、これらの電子は三つのd軌道を充足する形で、それぞれの軌道に2個ずつの電子が配置された閉塞場を呈しています。しかし、鉄がイオン化すると一番外側の第三d軌道電子が無くなり、鉄原子は2価の触手を持つ事になります。こうした鉄元素は「二価鉄」と呼ばれますが、そのニ価鉄が更にイオンした場合は今度は第二d軌道電子が1個奪われて二つの軌道磁界が誕生する事になります。同心面上に形成された二つの同極軌道磁界は磁束同士が反発し合って第二軌道磁界そのものが軌道面を大きく変化させる事になりますが、ニ価鉄が三価鉄もしくは四価鉄の触手を獲得した事になります。
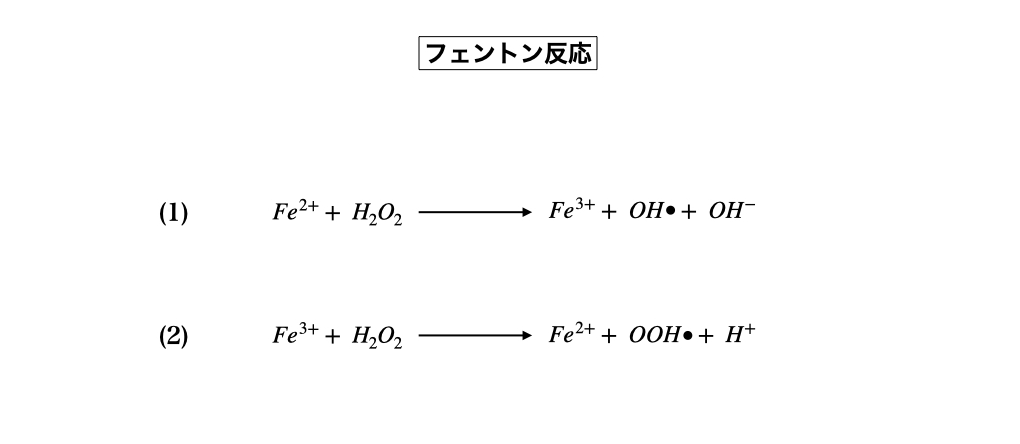
ちなみに、「フェントン反応」とは二価鉄(硫酸鉄: FeSO4)に過酸化水素(H2O2)を反応させて、三価鉄{硫酸鉄: Fe2(SO4)3}とハイドロキシ・ラジカル(OH・)を生み出す反応ですが、逆にその三価鉄に過酸化水素を反応させると三価鉄が二価鉄に戻って、その代わりにハイドロペルオキシラジカル(OOH・)が誕生してくるというラジカル育成反応です。これは過酸化水素が二価鉄から軌道電子を奪って三価鉄に変化させたり、また逆に三価鉄が過酸化水素から電子を奪い返して二価鉄へ戻る反応でしょうか。

さて、電子軌道の話から有機化学の話へ戻しますが、環式化合物の「ベンゼンC6H6」は平面的な亀の甲(六角形)構造を呈する有名な芳香族炭化水素であり、地球化学の分析ではベンゼン核を構成する6個の炭素は「sp2混成軌道」を取っていると言いますが、その言っている意味が我々には全然理解できない事から、ベンゼン骨格が如何様な電子軌道で結び付いているのか、宇宙科学の磁極結合論の方から説明したいと思います。下図がベンゼンの炭素結合の図ですが、磁極結合理論を用いれば誰もが簡単に納得できる回答が得られるのに、なぜ地球化学は難しく難しく考えるのでしょうか。「σ結合」とか「π結合」とか「sp2混成軌道」とか、一体何の意味なのでしょう。そもそも互いの電子を共有し合う現象が本当に存在するのか否か、これまで誰も確認できていないし、もし仮に電子を共有し合ったとしても、それが原子と原子の結合力と本当に関係するのかどうか、余りにも馬鹿げており、我々としては「もはや笑うしか無い」状況でしょうか。

その3に続く
【音声読み上げ】







Comments are closed